0512-67998889(苏州)
18051093220(深圳)
东风夜放花千树 | 九游中心生物泛肿瘤巨噬细胞药物阶段性成果发表
TME诱导的Tri-TRAIL巨噬细胞载体彰显非凡抗肿瘤威力,近期在肿瘤治疗领域取得重大突破。公司科研团队最新研发成果,题为“Tumor micro-environment induced TRAIL secretion from engineered macrophages for anti-tumor therapy”的论文,已在细胞免疫学领域国际期刊《Cellular Immunology》上发表,九游中心生物创始人尹秀山教授担任通讯作者。
TRAIL,全称为肿瘤坏死因子相关凋亡诱导配体,长期以来被视为极具潜力的肿瘤靶向治疗分子。然而,其在临床应用中的局限性一直未能得到妥善解决。为克服这一瓶颈,九游中心生物科研团队创新性地开发了Tri-TRAIL-iM巨噬细胞载体,这是一种能在肿瘤微环境(TME)特定条件下激活,精准释放三聚体TRAIL(Tri-TRAIL)的工程化巨噬细胞。Tri-TRAIL-iM的设计巧妙地利用了巨噬细胞的天然特性,使其成为TME响应式药物递送平台。在体外和动物模型中,Tri-TRAIL-iM展现出对肿瘤细胞的显著细胞毒性,同时对正常细胞影响极小,凸显了其在提高治疗效果和降低副作用方面的优势。
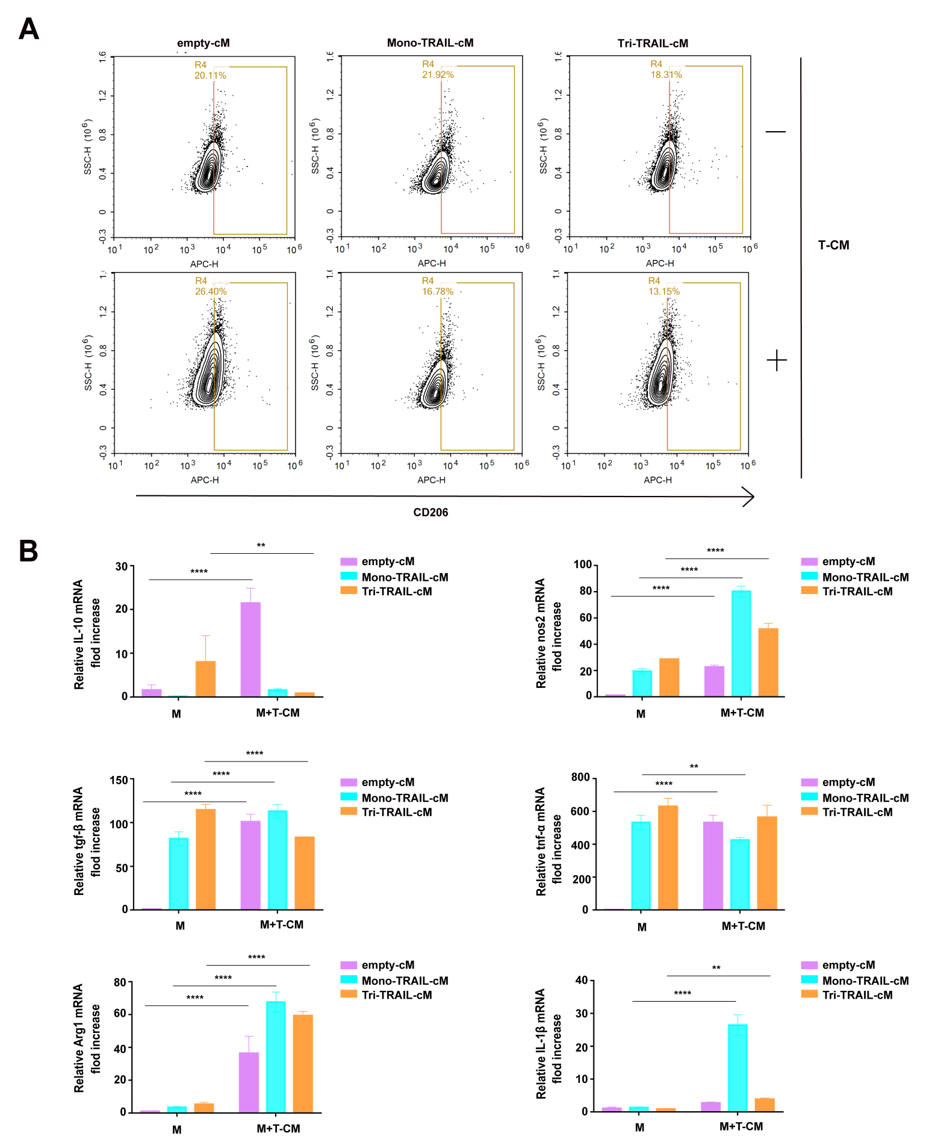
研究人员将小鼠成熟TRAIL与α1(I)胶原的人C肽融合,设计出了Tri-TRAIL-cM。通过Western Blot分析和流式细胞术验证,证实了RAW264.7细胞经慢病毒转导后能高效表达两种形式的TRAIL,其中Tri-TRAIL-cM的分泌水平明显高于Mono-TRAIL-cM。ELISA定量分析进一步确认了Tri-TRAIL-cM在细胞培养上清液中的浓度随时间增加,尤其在24小时后,其浓度显著高于Mono-TRAIL-cM。Annexin V/PI双染色法显示,TRAIL的分泌并未对载体细胞产生毒性。更深层次的表型研究表明,在TME诱导下,分泌TRAIL的巨噬细胞,特别是Tri-TRAIL-cM,能显著下调M2(促癌)表型标志物CD206的表达,同时抑制IL-10和TGFβ的转录活性。这些工程化巨噬细胞在TME中维持了促炎基因的活性,同时高表达Arg1,这与先前研究结果相符,突显了巨噬细胞在肿瘤免疫调控中的关键角色。
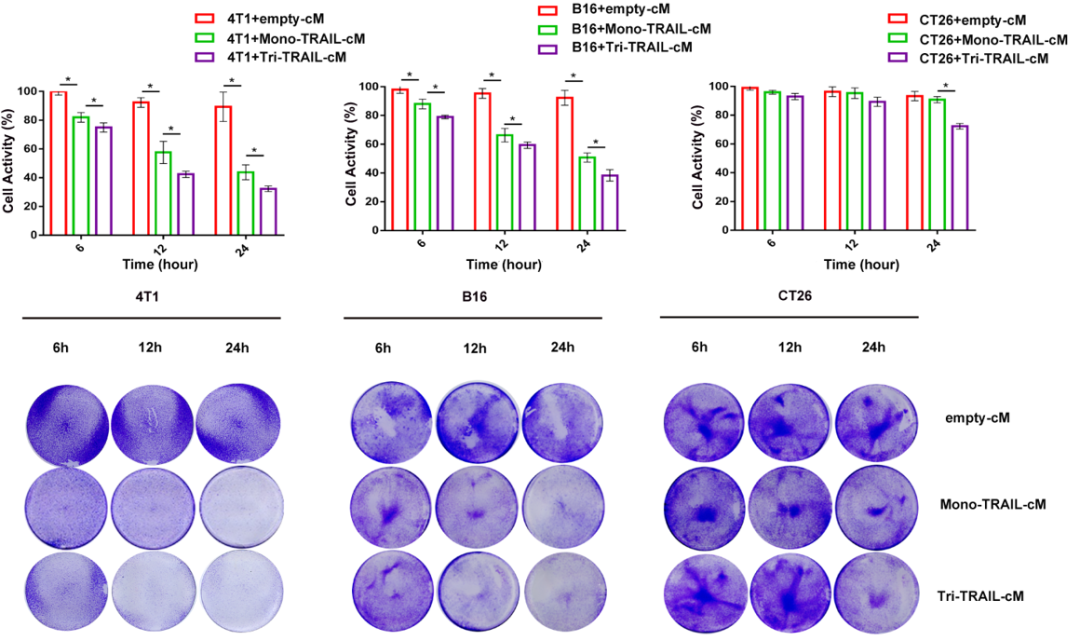
在体外细胞研究中,Tri-TRAIL-cM条件培养基对4T1、B16和CT26等肿瘤细胞均展现出不同程度增强的细胞毒活性。这一发现证实了Tri-TRAIL针对肿瘤细胞的高效促凋亡能力,特别是在共培养实验中,其对4T1细胞的凋亡诱导作用更为突出。
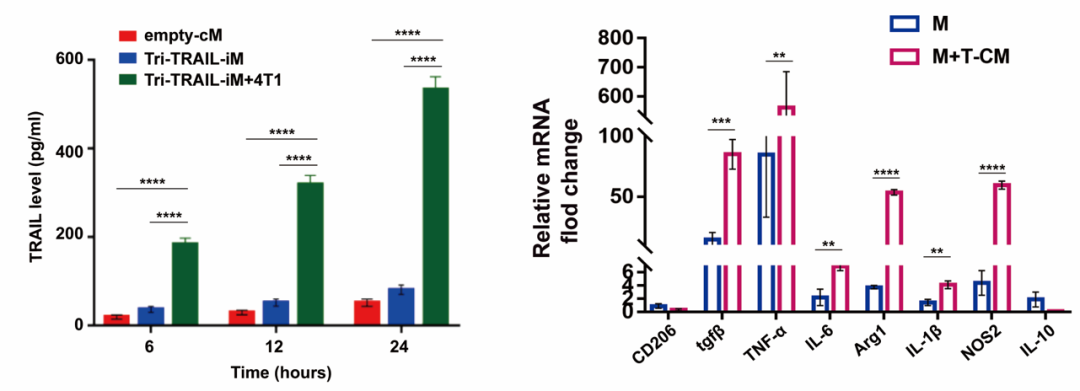
进一步地,团队利用Arg1启动子改造得到地Tri-TRAIL-iM,其在正常培养条件下TRAIL分泌水平较低,而在肿瘤调控介质(T-CM)诱导下,TRAIL水平显著升高,展现出对肿瘤微环境(TME)的特异性响应。在TME刺激下,Tri-TRAIL-iM不仅激活了促炎症基因的转录,还避免了非特异性细胞毒性,强化了其抗肿瘤效能。这一创新策略为提高癌症治疗的精准度和减少副作用提供了新途径。
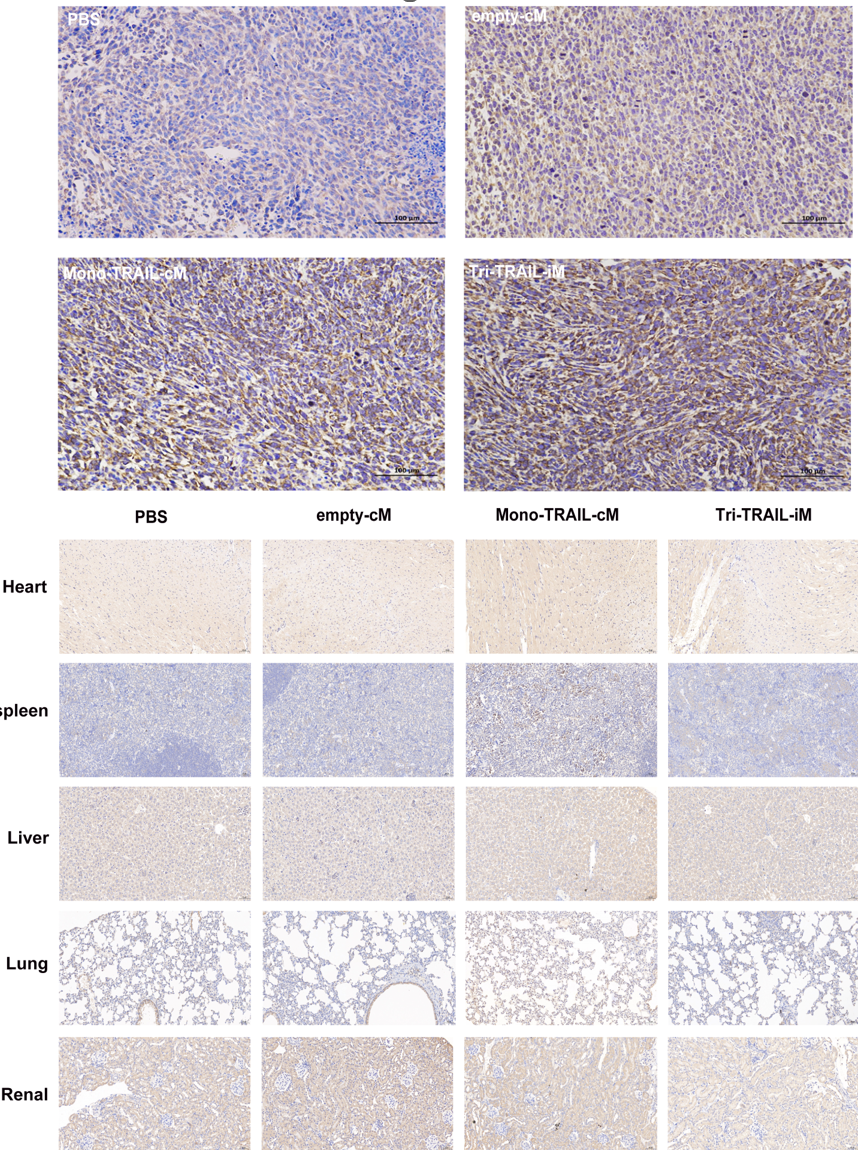
研究人员利用4T1细胞建立了小鼠皮下肿瘤模型,通过免疫染色法评估了Tri-TRAIL-iM在肿瘤和正常组织中的表达情况。实验结果显示,Tri-TRAIL-iM在肿瘤组织中诱导了高水平的TRAIL表达,与Mono-TRAIL-cM组相当。然而,不同于Mono-TRAIL-cM在多个正常器官中亦有TRAIL表达的现象,Tri-TRAIL-iM在非肿瘤组织中未观察到TRAIL的积累,体现了其出色的肿瘤特异性和减少非肿瘤组织副作用的潜力。
Tri-TRAIL-iM巨噬细胞载体在皮下肿瘤小鼠模型中同样展现出显著的抗肿瘤活性与卓越的治疗安全性。实验结果显示,接受Tri-TRAIL-iM治疗的小鼠肿瘤生长显著减缓,与PBS对照组和Mono-TRAIL-cM组形成了鲜明对比,不仅有效控制了肿瘤体积的增长,还在晚期阶段维持了小鼠体重稳定,凸显了其优越的治疗指数和安全性。
更深层次的组织学分析进一步揭示了Tri-TRAIL-iM治疗的多维益处。Tri-TRAIL-iM显著提升了肿瘤细胞的凋亡率,同时降低了Ki-67这一细胞增殖标志物的表达水平,表明其能够有效抑制肿瘤细胞的增殖。此外,Tri-TRAIL-iM还促进了iNOS阳性的促炎性巨噬细胞数量增加,这不仅反映了其对肿瘤微环境的积极重塑作用,还为理解其抗肿瘤机制提供了关键线索。
总而言之,九游中心生物的最新研究证实,巨噬细胞作为生物医学领域的一种高效药物递送平台,能够将Tri-TRAIL精准投递至肿瘤微环境,有效抑制实体瘤的进展。这一创新策略不仅显著增强了对肿瘤细胞的靶向杀伤力,诱导其凋亡,同时最大程度地保护了正常细胞,减少了治疗过程中的不良反应。将 Tri-TRAIL 与嵌合抗原受体工程化巨噬细胞(CAR-M)等先进疗法相结合,专门识别和攻击肿瘤细胞,可以协同抗击实体瘤。九游中心生物将持续深耕这一领域,以期为全球癌症患者带来革命性的治疗方案。
0512-67998889(苏州)
18051093220(深圳)

Cathy.Lv@mycoachlog.com(苏州)
lliangjing@mycoachlog.com (深圳)